Vanadin(V)oxid
I den här artikeln kommer vi att utforska effekterna och konsekvenserna av Vanadin(V)oxid på det moderna samhället. Från dess uppkomst till dess inflytande på olika aspekter av det dagliga livet har Vanadin(V)oxid spelat en avgörande roll för att forma olika områden, såsom politik, ekonomi, teknik och kultur. Genom en djupgående analys kommer vi att undersöka hur Vanadin(V)oxid har utvecklats över tid och hur det har format uppfattningar och handlingar hos människor runt om i världen. Dessutom kommer vi att ta upp de kontroverser och debatter som Vanadin(V)oxid har genererat, såväl som dess potentiella inverkan i framtiden. Denna artikel syftar till att ge en heltäckande och insiktsfull syn på Vanadin(V)oxid och dess betydelse i det samtida samhället.
| Vanadinpentoxid | |
  | |
| Systematiskt namn | Divanadin(V)pentoxid |
|---|---|
| Övriga namn | Vanadinpentoxid |
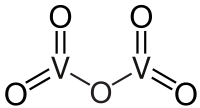
| Kemisk formel | V2O5 |
| Molmassa | 181,88 g/mol |
| Utseende | Gult till orangebrunt pulver |
| CAS-nummer | 1314-62-1 |
| SMILES | (=O)(=O)O(=O)(=O) |
| Egenskaper | |
| Densitet | 3,36 g/cm³ |
| Löslighet (vatten) | 8 g/l |
| Smältpunkt | 690 °C |
| Kokpunkt | 1750 °C (sönderfaller) |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| LD50 | 10 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
Vanadin(V)oxid eller vanadinpentoxid är en kemisk förening av metallen vanadin och syre med formeln V2O5.
Framställning
Vanadinpentoxid framställs ur vanadinmalm genom att behandla den med natriumkarbonat (Na2CO3) vilket ger salterna natriummetavanadat (NaVO3) och natriumortovanadat (Na3VO4). När svavelsyra tillsätts lösningen fälls olika oxider av vanadin ut när pH-värdet har fallit till runt 2. Utfällningen värms upp till 690 °C vilket ger vanadinpentoxid.
Användning
Den största mängden vanadinpentoxid används vid framställning av olika stål-legeringar. Den reduceras med kol eller koks i masugnsprocessen på samma sätt som järn(III)oxid.
Vanadinpentoxid används också vid tillverkningen av svavelsyra. Det är nämligen en effektiv katalysator för att oxidera svaveldioxid till svaveltrioxid.
Andra tillämpningar är som sensormaterial i bolometrar och värmekameror.
Se även
Källor
- Material Safety Data Sheet Mallinckrodt Baker
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Vanadium(V) oxide, tidigare version.

