Nitril
I dagens värld har Nitril blivit ett ämne av stor relevans och intresse för en bred publik. Oavsett om det är hans imponerande prestationer, kontroversiella handlingar eller historisk relevans, har Nitril fångat allmänhetens uppmärksamhet på en mängd olika sätt. Under årens lopp har Nitril varit föremål för intensiv granskning och studier, så att experter och entusiaster har kunnat utforska dess många aspekter och dimensioner. I den här artikeln kommer vi att fördjupa oss i den fascinerande världen av Nitril, utforska dess ursprung, evolution och återverkningar på dagens samhälle. Genom en detaljerad och omfattande analys kommer vi att upptäcka betydelsen och inverkan av Nitril i vårt dagliga liv och världen i stort.
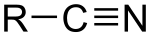
Ej att förväxla med nitrilgummi som ofta kallas "nitril".
Nitriler är kemiska organiska föreningar innehållande cyanogrupp (-C≡N). Om kolkedjan i stället binder till kvävet (-N≡C) fås en isonitril. Nitriler kan i en viss mening ses som organiska cyanider och vissa kan under omständigheter frisätta den mycket giftiga cyanidjonen (CN-). Nitriler har många användningsområden och förekommer dels naturligt i flera föreningar från växt- och djurriket samt i av människan syntetiserade föreningar.
Syntes av nitriler
Det finns flera sätt att framställa nitriler.
- SN2 av alkylhalider med metallcyanider, till exempel kaliumcyanid.
- Dehydratisering av primära amider, vanligen med fosforpentoxid.
- Dehydratisering av aldoximer, vanligen med ättiksyraanhydrid.
- Primära aminer med ett primärt kol kan oxideras till motsvarande nitril. Vanliga oxidationmedel i denna process är bly(IV)acetat och natriumhypoklorit.
- Arylhalider ger med vattenfri kopparcyanid motsvarande arylnitril. Denna syntes kallas Rosenmund-von Braun-reaktionen.
- Arylaminer (aniliner) kan genom behandling med salpetersyrlighet ge diazoniumjoner, vilka vid behandling med kopparcyanid ger motsvarande nitril i en så kallad Sandmeyersyntes.
Reaktioner med nitriler
Nitriler är viktiga syntesintermediärer.
- Nitriler kan surt eller basiskt hydrolyseras tillbaka till motsvarande karboxylsyra. Denna process är dock relativt långsam och kräver många gånger höga temperaturer och långa reaktionstider.
- Nitriler kan reduceras till aldehyder (under kontrollerade former) eller till aminer. Vanligen används litiumaluminiumhydrid eller DIBAL.
- Nitriler reagerar med Grignardreagens under bildande av motsvarande keton.
| |||||||||||||||||||||||||||||||||